Geradores de Microbolhas para incorporar ozônio na água
Geradores de Microbolhas para incorporar ozônio na água

Os geradores de microbolhas são, sem dúvida nenhuma, a melhor tecnologia para incorporar o ozônio em meio aquoso para a indústria de alimentos. Microbolhas e nanobolhas são bolhas de gás extremamente pequenas que possuem várias propriedades físicas únicas que as tornam muito diferentes das bolhas normais. Essas propriedades tornam as microbolhas e as nanobolhas um método de aeração superior para uma série de aplicações em todo o mundo.
A injeção no meio aquoso por meio da tecnologia microbolhas aumenta de forma exponencial a eficiência do processo. Uma microbolha que possui tamanho de 0,5 a 5 micras (500 à 2.000 vezes menor que 1 centímetro) e a nanobolha possui tamanho de 0,0005 a 0,001 micras (1.000.000 vezes menor que 1 centímetro). Quanto menores forem as bolhas, maior será o tempo de contato com a água e isso melhora exponencialmente as chances de incorporação do ozônio na solução aquosa. Pesquisas científicas estimam que em um metro cúbico de microbolhas possuem, quando somadas, uma superfície de contato de aproximadamente de 200km².

Geradores de microbolhas desenvolvidos no Brasil pela empresa myOZONE® (a) e (b) ao lado de um reservatório de 500L (c) após 2 minutos de funcionamento do gerador de microbolhas da myOZONE
As principais propriedades das microbolhas e nanobolhas são:
Empuxo Neutro: As microbolhas diâmetro de 1.000nm e as nanobolhas têm um diâmetro médio típico de cerca de 80nm. As bolhas nestes dois tamanhos não têm flutuabilidade suficiente para alcançar a superfície e, em vez disso, seguem o movimento browniano no reservatório. O resultado é que as microbolhas e nanobolhas permanecerão submergidas na água por horas (microbolhas) ou semanas (nanobolhas) até serem consumidas pelo meio líquido. Enquanto isto não acontece, as bolhas viajam aleatoriamente por todo o corpo d’água e solubilizando com maior eficiência. Após um tempo, o ozônio dissolvido medido nas partes mais profundas de um tanque ou reservatório irá corresponder ao ozônio dissolvido registrado próximo à superfície homogeneizando melhor todo o meio líquido.
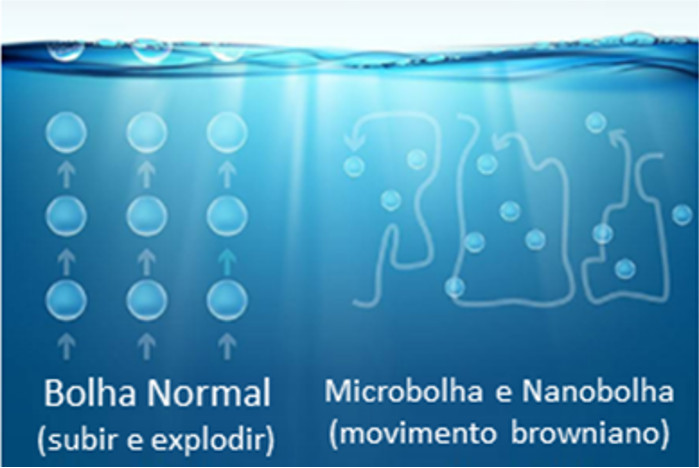
Fonte: Nanobubble Systems
Carga de superfície: Todas as bolhas possuem naturalmente uma carga elétrica superficial. Quanto menor a bolha, mais forte é a carga superficial. As nanobolhas têm um alto potencial zeta, que é o potencial eletrocinético em dispersões coloidais. Diversos estudos científicos demonstram que a forte carga negativa das nanobolhas limita sua coalescência, o que significa que a integridade da bolha é preservada em qualquer profundidade por longos períodos. Além disso, a carga negativa combinada com sua alta concentração melhora a eficiência de separação em processos de flotação, aumentando a probabilidade de colisão. Já a microbolha possui a mesma propriedade, porém em escala menor que uma nanobolha.
Reserva de gás: A flutuabilidade neutra e a carga superficial negativa das microbolhas permitem que permaneçam em suspensão por várias horas, já as nanobolhas permitem que elas permaneçam em suspensão por semanas a fio. Isso ocorre mesmo depois que a solução atinge a saturação de ozônio. Nessa capacidade, as microbolhas e nanobolhas atuam como reserva de gás na solução. À medida que o ozônio é consumido da água pela biologia, química ou liberação de gases, as microbolhas e nanobolhas rapidamente difundem mais ozônio na água, mantendo elevados níveis de ozônio dissolvido até que as microbolhas e nanobolhas se esgotem. Essa reserva adicional de gás, estimada em até 20% acima do ponto de saturação, permite que as indústrias utilizem o ozônio de forma mais econômica e eficiente.
Eficiência de transferência de ozônio: Um requisito fundamental de qualquer aplicação onde se busca a transferência eficiente de ozônio para um meio líquido. Os sistemas de aeração convencionais transferem apenas 1% a 3% de ozônio por metro cúbico de água devido ao seu tamanho e à taxa de aumento rápida correspondente. Isso torna a aeração convencional altamente ineficiente. A tecnologia de microbolhas e nanobolhas aproveitam as suas propriedades exclusivas e oferecem uma eficiência de transferência de ozônio podendo chegar a uma solubilidade de 90-95% por metro cúbico de água. A longevidade das microbolhas e nanobolhas na água, juntamente com sua alta área de superfície por volume, torna-as o método de solubilidade mais eficiente do mercado atualmente e permite as instalações serem menores e mais eficientes.
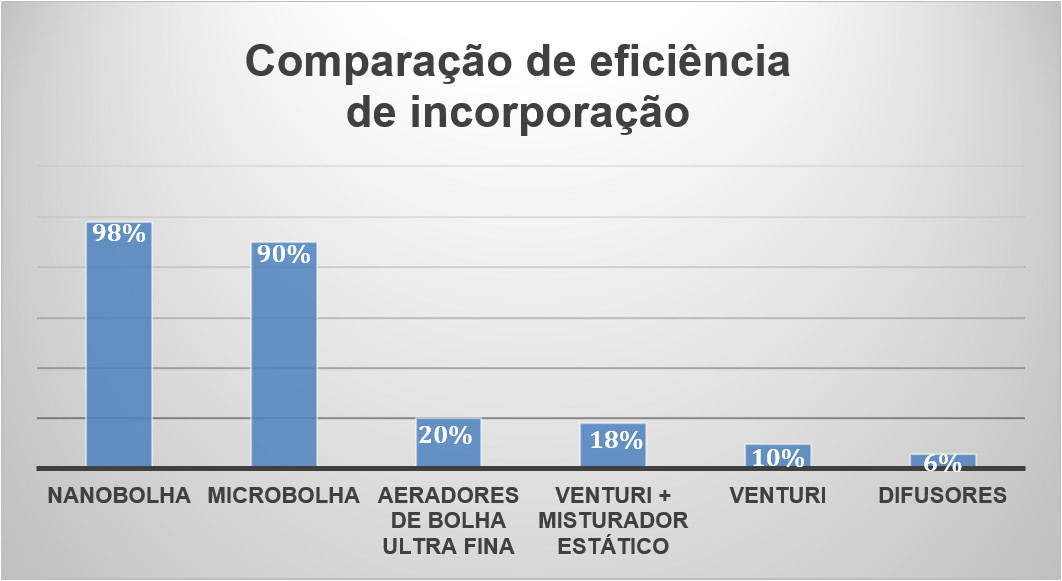
Eficiência de incorporação entre as tecnologias existentes. Fonte: myOZONE
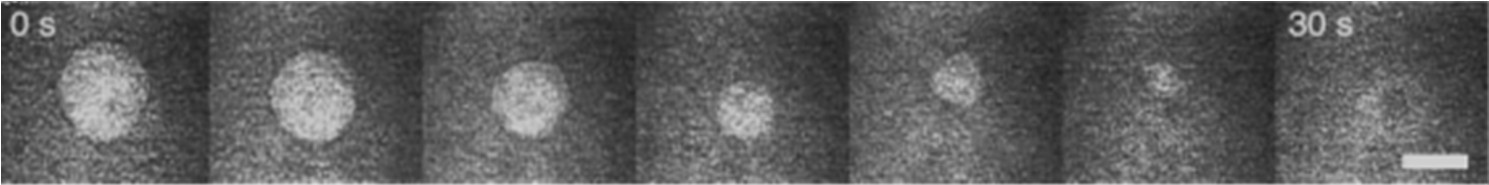
Incorporação de uma microbolha de ozônio analisada por microscópio eletrônico. fonte myOZONE
Tamanho da bolha: Nanobolhas são o menor tamanho de bolha conhecido, 500 vezes menor que uma microbolha ou aproximadamente do tamanho de um vírus. Nessa escala, muito mais nanobolhas podem caber no mesmo volume de água em comparação com outras bolhas. Eles também têm várias características exclusivas diretamente relacionadas ao seu tamanho em miniatura, que incluem flutuabilidade neutra, uma forte carga elétrica e uma alta eficiência de transferência. Bolhas maiores não possuem essas características, o que as torna menos benéficas em uma série de aplicações quando comparadas às microbolhas e nanobolhas.

Eficiência de incorporação entre as tecnologias existentes
Fonte: Nanobubble Systems
Superfície: As nanobolhas têm mais de 400 vezes a área de superfície de uma microbolha típica de 40 micrômetros de diâmetro. A maior área de superfície de contato da microbolha sobre uma bolha comum permite maior transferência de massa, garantindo que praticamente que o ozônio seja efetivamente entregue à água. Estima-se que dentro de 1 única microbolha cabem 64 milhões de nanobolha. Cada nanobolha possui tamanho aproximado de um vírus.
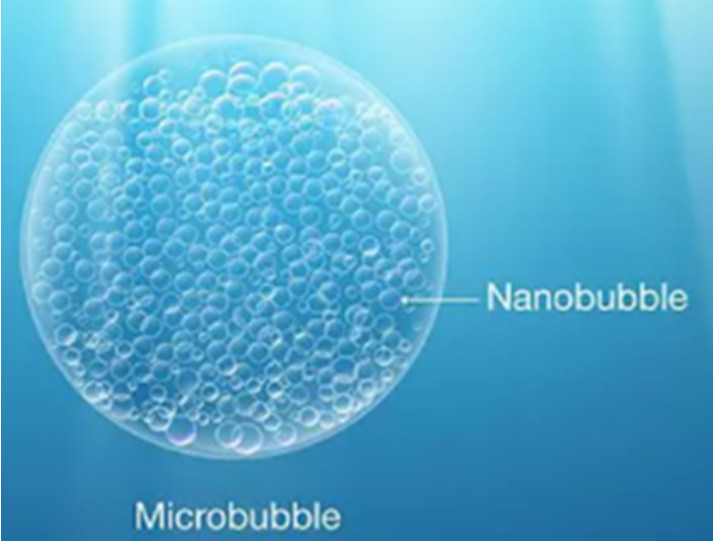
Área de superfície de contato Nanobolha.
Fonte: Nanobubble Systems.
A decomposição do ozônio na água é caracterizada por uma diminuição de concentração diluída inicial rápida devido às reações de oxidação dos materiais presentes na solução aquosa, seguida por uma segunda fase na qual ozônio aumenta a concentração. As reações que ocorrem não são fáceis de explicar, não só porque muitas reações químicas podem ocorrer simultaneamente, mas também porque o ozônio pode reagir indiretamente (decomposição através de um mecanismo de reação em cadeia, resultando na produção de hidroperóxidos, superóxidos e hidroxilas livres e radicais) ou diretamente via reações seletivas com substâncias na matriz água.
Processos de reação do ozônio na água
Este efeito combinado torna o ozônio um dos oxidantes mais eficientes quando comparado a outros produtos químicos. Portanto, a eficácia de um processo de ozonização baseia-se geralmente sobre os efeitos de ambos os mecanismos de reação direta e indireta, e em grande parte dependem da composição química da água, sua temperatura e especialmente seu pH, o tipo e conteúdo de matéria orgânica.
A incorporação do ozônio na água em radicais de hidroxila OH– (moléculas com um elétron não pareado), surge a partir da reação via indireta. É amplamente conhecido que os radicais OH resultantes desta reação são compostos de muito curta duração que tem um potencial de oxidação ainda mais forte do ozônio porque os radicais são altamente instáveis e imediatamente se reagem com outra molécula para recuperar o elétron faltando.
O processo de oxidação provocado pelo ozônio pode ser muito complexo: Pode ser resumido a um conjunto de reações indiretas que levam à formação de vários elementos.
- Fase de Iniciação: A reação entre o íon hidroxila e o ozônio leva a formação do ânion radical superóxido O2– e do radical hidroperoxila HO2• :
| O3 + OH– → O2•- + HO2• |
O radical hidroxila apresenta um equilíbrio ácido-base:
| HO2 → O2•- + H+ |
- Fase de Propagação: O ânion radical de ozônio (O3–) formado da reação entre o ozônio e o ânion radical superóxido (O2•-) decompõe-se, muito rapidamente, para formar os radicais hidroxila e oxigênio.
| O3•- + O2•- → O3•- + O2 | |
| HO3• O3•- + H+ | |
| HO3• → OH• + O2 |
O radical de hidroxila (OH•) pode reagir com o ozônio da seguinte maneira:
| OH• + O3 → HO4• | |
| HO4• → O2 + HO2• |
Com o decaimento de HO4• para O2 e HO2• a reação em cadeia pode começar de novo. Substâncias que convertem OH• para radicais superóxidos O2• e/ou hidroperóxidos HO2• promovem a reação em cadeia e, devido a isto, são chamadas de promotoras. As moléculas orgânicas, R, também podem agir como promotoras.
H2R + OH• → HR• + H2O
Se o oxigênio está presente, radicais orgânicos peróxido ROO• podem ser formados. E estes podem reagir em seguida, eliminando O2•-/HO2• e entrando na reação em cadeia.
HR• + O2 → HRO2•
HRO2 • → R + HO2•
HRO2• → RO + OH•
Fase de Terminação: Algumas substâncias orgânicas e inorgânicas reagem com o radical de hidroxila e formam radicais secundários que não produzem O2– / HO2-•, atuando como inibidores das reações em cadeia.
OH• + CO3 2- → OH– + CO3•-
OH• + HCO3– → OH– + HCO3•
Outra possibilidade para reação de terminação é a reação entre dois radicais:
OH• + HO2• → O2 + H2O
A combinação destas reações mostra que três moléculas de ozônio produzem dois radicais hidroxilas:
3O3 + OH– + H+ → 2OH• + 4O2
O radical de hidroxila é um dos radicais livres mais reativos e um dos agentes oxidantes mais fortes que se tem notícia (E0 ≅ 2,7 V). Outra característica dos radicais de hidroxila, que os torna muito eficientes para degradar compostos poluentes, é sua rápida cinética de reação; para compostos orgânicos observam-se constantes entre 106 e 1010L mol-1 s-1 (ou seja, atingem valores da mesma ordem de grandeza da constante de difusão do OH em meio aquoso, kdif = 7 x 109 L mol-1 s-1). Além disso, essa molécula é bem menos seletiva que o ozônio, sendo capaz de oxidar uma ampla gama de compostos.
Processo Oxidativo Avançado – POA
Devido a estas vantagens, o emprego do ozônio visa a formação de radicais de hidroxila (ou seja, atuando como um Processo Oxidativo Avançado – POA) é muito mais versátil e costuma ser a forma mais empregada, principalmente por ser muito eficiente para promover a completa oxidação (mineralização) dos compostos orgânicos poluentes.
Várias abordagens podem ser utilizadas com este intuito, dentre elas destacam-se o uso combinado do ozônio com: radiação UV, peróxido de hidrogênio (H2O2), ultra-som, catalisadores óxido-metálicos (ex: óxido de titânio e óxido de manganês), etc. A variação do pH costuma ser a abordagem mais simples (embora não a mais eficiente) para se obter mais geração de radicais hidroxila a partir do ozônio.
Geralmente, sob condições ácidas (pH≤4) o mecanismo direto (reação do ozônio) predomina, acima do pH 10 ele se torna predominantemente indireto (reações radiculares). Para águas naturais (superficiais ou subterrâneas) com pH 7, ambos mecanismos podem estar presentes e outros fatores (como tipo do composto alvo e presença de metais de transição) contribuirão para definir a extensão de cada um deles.
Vários exemplos mostram que o ozônio reage de forma direta ou indireta apresentando bons resultados na desinfecção de águas para consumo humano e na degradação de uma série de compostos poluentes presentes em águas naturais e/ou efluentes (principalmente os oriundos das indústrias químicas e alimentícias).
Além da esterilização de uma série de microrganismos patogênicos, os efeitos benéficos do ozônio são mais pronunciados na remoção de cor (devido à degradação/oxidação de grupos cromóforos) e formação de moléculas menores, com maior hidrofilicidade (capacidade de solubilizar em água) e menor toxicidade, pois as etapas oxidativas tendem a fragmentar macromoléculas poluentes.
Geralmente tais transformações contribuem para aumentar a biodegradabilidade dos compostos recalcitrantes aos tratamentos biológicos (transformação/oxidação dos poluentes a produtos mais facilmente metabolizados pelos microrganismos). Embora alguns estudos mostrem que os processos de ozonização também podem promover certa redução na demanda química de oxigênio (DQO), demanda bioquímica de oxigênio (DBO) e no teor de carbono orgânico total (COT), geralmente os níveis de redução de matéria orgânica são menores que os obtidos com outros POAs ou necessitam de um dispêndio maior de reagentes e/ou energia, tornando-os sozinhos desfavoráveis do ponto de vista econômico.
Assim, recomenda-se utilizar o ozônio na etapa final de um processo de tratamento convencional, devido a essas limitações. Vários estudos estão sendo realizados buscando-se aumentar a eficiência dos processos de oxidação por ozônio, principalmente com relação às taxas de mineralização dos compostos orgânicos poluentes.
Vantagens dos processos avançados de oxidação
Devido a seletividade do ozônio molecular, nem todos os compostos em uma solução de água são rapidamente oxidados por ele e certamente não às mesmas taxas. Além disso, além do fato de que o ozônio tem relativamente baixa solubilidade e estabilidade na água, às vezes a própria água pode conter compostos resistentes ao ozônio, como muitos pesticidas, antioxidantes e solventes clorados.
Portanto, como resultado do custo de produção de ozônio e a oxidação parcial de compostos mais orgânicos presentes na água, a aplicação do ozônio pode parecer não ser viável do ponto de vista econômico. Uma maneira de superar esse problema é transformar e aumentar a camada de radicais de hidroxilas e hidroperóxidos muito mais reativos que o próprio ozônio, em um procedimento conhecido como “processo de oxidação avançada”.
Este termo simplesmente define um processo de oxidação que gera os radicais OH em grandes quantidades, a fim de aumentar o nível de tratamento de soluço aquosa. Estes radicais podem ser iniciados na água contendo ozônio por meio de um ativador, como o peróxido de hidrogênio (H2O2) e radiação ultravioleta (Lâmpada UV) ou catalizadores como óxido de manganês, óxido de titânio, sais de ferro e etc. Então, devido aos processos de oxidação, substâncias nocivas são decompostas em substâncias menos nocivas, sem a formação de partículas em suspensão.
Ao longo dos anos, processos avançados de oxidação (POA) têm sido usados para produzir radicais OH para degradar com sucesso mais cargas orgânicas presentes na água poluída.
No entanto, porque os radicais OH são mais poderosos oxidantes que ozônio molecular, e por causa de suas reações não seletivas, eles também são susceptíveis de serem utilizados por reações competitivas.
A eficiência desses métodos se deve principalmente pela imobilização de hidrocarbonetos perfluorados, que impede a dissolução de moléculas perfluorados em fase aquosa, usando uma técnica que envolve o líquido-líquido extração de substâncias orgânicas da fase aquosa para a fase orgânica e subsequente oxidação por ozônio molecular dissolvido na fase orgânica (apolares perfluorados solvente hidrocarboneto saturado com ozônio).
A escolha de um profissional experiente para projetar e orientar a instalação são de importância primordial no sucesso e segurança da instalação.






